電食という言葉をご存知でしょうか。
電食はガルバニック腐食とも呼ばれ、異なる金属が接している時に起こる腐食のことを言います。
例えば、銅材を亜鉛メッキボルトで固定していると亜鉛めっきボルトが腐食するなどです。
ではなぜ亜鉛メッキボルトがなぜ錆びるのでしょうか。
それはイオン化傾向に関係しています。
イオン化傾向の大きい金属と小さい金属が接している箇所に、電解質を含む液体が(塩水等)が存在すると電流が生じます。
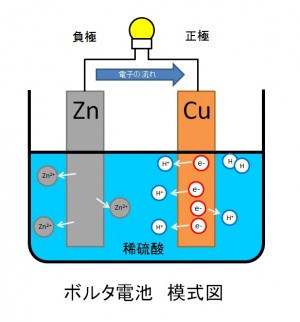
イオン化傾向が大きい金属が負極、イオン化傾向が小さい金属が正極となります。負極とな る金属は電解質を含む液体にイオン化して溶け出し、腐食するというメカニズムです。
銅材と亜鉛メッキボルトの場合はイオン化傾向の大きい亜鉛が負極となり、銅が正極となります。亜鉛が溶け出し、メッキが無くなってしまい生地の鉄等が錆びてしまいます。
これはボルタ電池と同じ現象になります。
イオン化傾向は、
・ 貸そう(K)か(Ca)な(Na)、ま(Mg)あ(Al)当(Zn)て(Fe)に(Ni)すん(Sn)な(Pb)ひ(H)ど(Cu)す (Hg)ぎる(Ag)借(Pt)金(Au)
・ リ(Li)カ(K)バー(Ba)する(Sr)か(Ca)な(Na)、曲(Mg)がる(Al)前にあえ(Zn)て苦労(Cr)して(Fe)カ ド(Cd)っこ(Co)に(Ni)すん(Sn)な(Pb)、ひ(H)ど(Cu)す(Hg)ぎ銀(Ag)座パー(Pt)キン(Au)グ
色々な語呂での覚え方があるようですが、イオン化傾向順に並べるとこのようになります。
イオン化傾向大 >>> リチウム > カリウム > バリウム > ストロンチウム > カルシウム > ナトリウム >マグネシウム > アルミニウム > マンガン > 亜鉛 > クロム > 鉄 > カドミウム> コバルト > ニッケル > スズ > 鉛 > 水素> 銅 > 水銀 > 銀 > 白金 > 金 >>> イオン化傾向小
イオン化傾向の大きい金属ほど反応性が高く、イオン化傾向の小さい金属ほど反応性が低くなります。
このイオン化傾向の差(電位差)が大きければ大きいほど、より大きな電気が流れ、その分腐食してしまいます。
では電食を起こさないようにするにはどのようにすれば良いのでしょうか。
電食を起こさないようにするには、
①同じ材料を使用する。
②電位差の小さい材料を使用する。
③メッキにより電位差を小さくする。
④樹脂などにより絶縁する。
などがあります。
下記リンクでは電食の仕組みを図解して解説しています。また、対策案についてもご紹介しています。
 |
電食防止のための表面処理 ガルバニック腐食(異種金属接触腐食)は異種金属が接触する事で発生しますが、その発生メカニズムに関してはそれぞれの金属の持つ標準電極電位の違いから起こる事が知られています。 ここではガルバニック腐食について図解して説明しています。 |
|---|
錆びにくいようにするには、材料、メッキ、使用環境などを考慮して最適な選択をする必 要があります。選択の際に迷われたり、
不明な点がありましたらメッキ.comまでお問い合わせ下さい。
今回はこれで以上です。
第100回 異種金属と電気化学的電位の関係を徹底解説!メッキの役割とは?
異種金属と電気化学的電位の関係を徹底解説!メッキの役割とは? 第100回を記念して、製品設計に役立つ、異種金属組み合わせ影響が一目でわかる「異種金属間の電位表」を無料進呈中